上海金畔社生物科技有限公司日本同仁化学dojindo全线产品代理 中国代理商
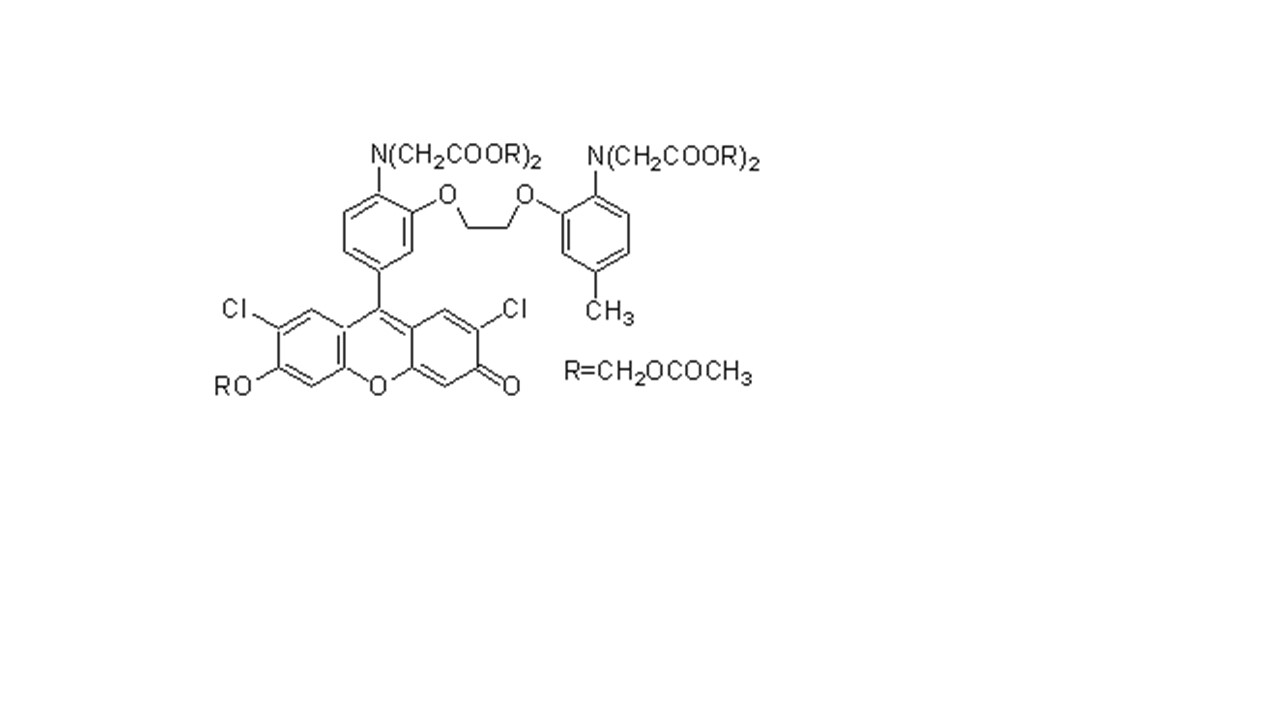
C51H50Cl2N2O23
1129.85
特点:
● 激发波长480-500 nm,发射波长523-530 nm
● 激光共聚焦,流式细胞仪均可检测

产品性状
规格
性状 : 本产品为红色粉末,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图: 符合实验要求
NMR光谱图: 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
Fluo 3-AM是一种检测细胞内钙离子的荧光探针。Fluo 3若以游离配体形式存在时几乎是非荧光性的,但是当它与钙离子Ca2+结合后荧光会增加60至80倍,是目前最常用的一种钙离子荧光探针。激光共聚焦荧光显微镜具有氩激光器,所以Fluo 3可被广泛使用于这种显微镜上。这种荧光信号发出来的长波也便于减小对样品细胞的光损伤。Fluo 3也可用来检测紫外光照射下可裂解的螯合钙或其它形式的钙。Fluo 3-AM是Fluo 3的一种乙酰甲酯衍生物,通过培养,能够轻易进入细胞中。
原理
Fluo 3-AM (钙离子荧光探针) 需用无水DMSO (anhydrous DMSO)配制。Fluo 3-AM是一种可以穿透细胞膜的荧光染料。Fluo 3-AM进入细胞后可以被细胞内的酯酶剪切形成Fluo 3,从而被滞留在细胞内。Fluo 3可以和钙离子结合,结合钙离子后可以产生较强的荧光,最大激发波长为506nm,最大发射波长为526nm
激发发射波长
E x :480-500 nm
Em:525-530 nm
操作步骤
1、用 HBSS 溶液稀释 1-5 mmol/l 的 Fluo 3-AM 母液,配制成 1-5 µmol/l的 Fluo 3-AM 工作液
(此浓度仅供参考,请根据具体实验要求自行调整)。
例如:1 mmol/l 母液配制 1 ml 浓度为 5 µmol/l工作液的方法:用 1 ml HBSS 溶液稀释 5 µl母液
即可。Fluo 3-AM 工作液需要即配即用,请勿反复冻存。如果Fluo 3-AM进入细胞的效果不好,
可使用Pluronic® F-127,后者可以防止Fluo 3-AM在缓冲液里聚合并能促进其进入细胞。
*Pluronic® F-127先用DMSO溶解至浓度为 20%(W/V),然后根据实验需要直接加入Fluo 3-AM工作液
中至终浓度为 0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,用 HBSS 溶液洗涤细胞 3 次。
如果使用含血清的培养基,血清中的酯酶会分解 AM 体,从而降低 Fluo 3-AM 进入细胞的效果。
另外含有酚红的培养基会使本底值略微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入 Fluo 3-AM 工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育10-60分钟,除去Fluo 3-AM工作液。关于孵育的时间,如果首次做实验不能定,
建议先孵育 30 分钟,看荧光效果:如果细胞死亡较多,适当缩短时间;如果荧光强度太弱,
适当延长时间。
5、用 HBSS 溶液洗涤细胞 3 次以充分去除残留的 Fluo 3-AM 工作液。然后加入 HBSS 溶液覆盖细胞。
6、37℃培养箱孵育约 20-30 分钟,以确保 AM 体在细胞内的完全去酯化作用。
如果细胞内酯酶活性较低,建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用激光共聚焦或荧光显微镜检测细胞,激发波长 480-500 nm,发射波长 525-530 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致AM体水解,荧光染料无法进入细胞,影响实验效果
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成5 μl/管,用封口膜封口,并用铝
箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件
实验案例
加载了Fluo 3的新鲜分离的大鼠肝脏细胞PE刺激后出现规则胞浆钙振荡。
上图为细胞明场图和不同时间点(min)的比例成像,
下图为影响Fluo 3荧光强度随时间的变化。
成像系统:Photon Technology International Inc.,
显微镜Nikon TE2000U,CCD相机QuantEM512S,软件ERP。
(北京师范大学细胞生物学研究所 崔宗杰教授 提供照片)
数据分析
计算公式:
[Ca2+]i = Kd×(F-Fmin) / (Fmax-F)
[Ca2+]i :细胞内Ca2+浓度
Kd:解离常数
F :荧光强度
Fmin:Ca2+为零状态下测得的荧光比值
Fmax:Ca2+为饱和状态下测得的荧光比值
文献
1) A. Minta, J. P. Y. Kao and R. Y. Tsien, “Fluorescent Indicators for Cytosolic Calcium Based on Rhodamine and Fluorescein Chromophores”, J. Biol. Chem., 1989, 264(14), 8171.
2) J. P. Kao, A. T. Harootunian and R. Y. Tsien, “Photochemically Generated Cytosolic Calcium Pulses and Their Detection by Fluo-3”, J. Biol. Chem., 1989, 264, 8179.
3) M. Eberhard and P. Erne, “Kinetics of Calcium Binding to Fluo-3 by Stopped-Flow Fluorescence”, Biochem. Biophys. Res. Commun., 1989, 163, 309.
4) A. Hernandez-Cruz, F. Sala and P. R. Adams, “Subcellular Calcium Transients Visualized by Confocal Microscopy in a Voltage-clamped Vertebrate Neuron”, Science, 1990, 247, 858.
5) A. H. Cornell-Bell, S. M. Finkbeiner, M. S. Cooper and S. J. Smith, “Glutamate Induces Calcium Waves in Cultured Astrocytes: Long-Range Glial Signaling”, Science, 1990, 247, 470.
6) D. A. Williams, “Quantitative Intracellular Calcium Imaging with Laser-scanning Confocal Microscopy”, Cell Calcium, 1990, 11, 589.
7) D. A. Williams, S. H. Cody, C. A. Gehring, R. W. Parish and P. J. Harris, “Confocal Imaging of Ionised Calcium in Living Plant Cells”, Cell Calcium, 1990, 11, 291.
8) P. A. Vandenberghe and J. L. Ceuppens, “Flow Cytometric Measurement of Cytoplasmic Free Calcium in Human Peripheral Blood T Lymphocytes with Fluo-3, A New Fluorescent Calcium Indicator”, J. Immunol. Methods, 1990, 127, 197.
10) M. Iino, H. Kasai and T. Yamazawa, “Visualization of Neural Control of Intracellular Ca2+ Concentration in Single Vascular Smooth Muscle Cells in situ”, EMBO J., 1994, 13 (21), 5026.
11) M. E. Dailey and S. J. Smith, “Spontaneous Ca2+ Transients in Developing Hippocampal Pyramidal Cells”, J. Neurobiol., 1994, 25(3), 243.
12) M. Burnier, G. Centeno, E. Burki and H. R. Brunner, “Confocal Microscopy to Analyze Cytosolic and Nuclear Calcium in Cultured Vascular Cells”, Am. J. Physiol., 1994, 266, C1118.
13) E. Donnadieu and L. Y. W. Bourguignon, “Ca2+ Signaling in Endothelial Cells Stimulated by Bradykinin: Ca2+ Measurement in the Mitochondria and the Cytosol by Confocal Microscopy”, Cell Calcium, 1996, 20 (1), 53.
14) M. Ikeda, H. Ariyoshi, J. Kambayashi, K. Fujitani, N. Shinoki, M. Sakon, T. Kawasaki and M. Monden, “Separate Analysis of Nuclear and Cytosolic Ca2+ Concentrations in Human Umbilical Vein Endothelial Cells”, J. Cell. Biochem., 1996, 63 (1), 23.
15) J. E. Merritt, S. A. McCarthy, M. P. A. Davies and K. E. Moores, “Use of fluo-3 to Measure Cytosolic Ca2+ in Platelets and Neutrophils Loading Cells with the Dye, Calibration of Traces, Measurements in the Presence of Plasma, and Buffering of Cytosolic Ca2+”, Biochem. J., 1990, 269, 513.
Q&A
|
Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
|
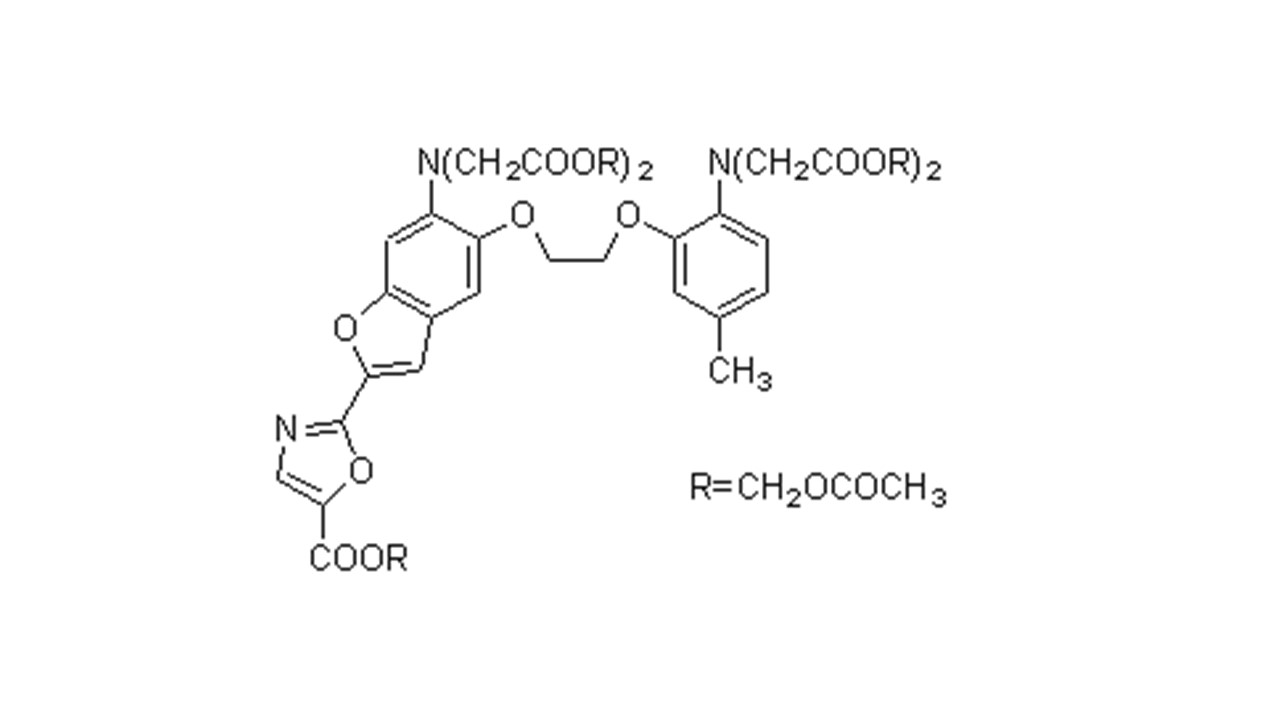
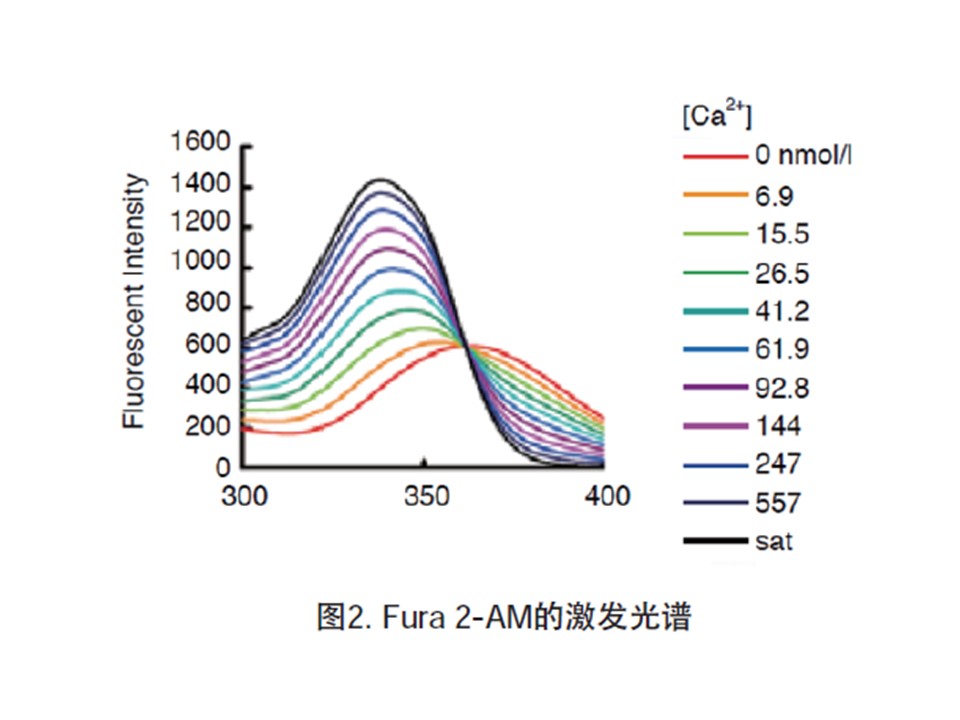
A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的 有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |