荧光计的工作原理
荧光计是用于精确定量微升 (μL) 样品中的各种生物分子(例如核酸和蛋白质)*工具。这些仪器在生命科学、环境监测、药品质量控制和生物工程应用等广泛的生化领域发挥着至关重要的作用。通过提供高灵敏度测量,荧光计能够对亚皮克浓度的样品进行定量。这篇博文将探讨荧光计的工作原理,阐明其基本机制并强调其在科学研究和分析中的重要性。
了解荧光计的功能
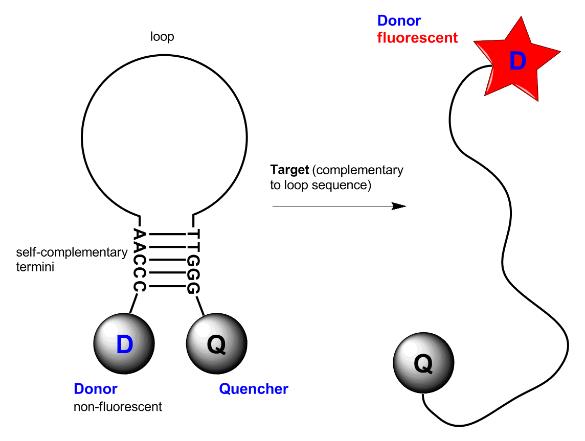
荧光计的工作原理是根据荧光对生物分析物进行定量。要开始该过程,需要将感兴趣的样品与特定的荧光剂结合,并使用聚丙烯管将其装入仪器中。有许多市售荧光试剂,包括核酸染料、细胞功能染料和荧光蛋白,使科学家能够根据自己的特定需求定制实验。
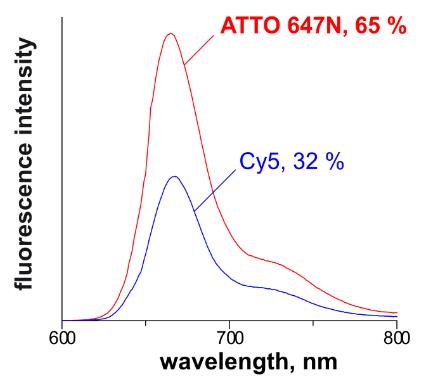
荧光团具有吸收特定激发波长的光并随后以较低的能量发射或发出更长波长的光的能力。某些荧光团在与特定分析物(例如双链 DNA (dsDNA))结合时会增强荧光。通过直接将检测的荧光强度 (RFU) 与样品中所需生物分子的数量相关联,科学家可以准确测量它们的浓度。
荧光测定的灵敏度
荧光测定法是一种极其灵敏的方法,能够以低至 0.0005 纳克/微升 (ng/μL) 的灵敏度检测生物分子。此外,荧光测定法可为所需分析物提供检测,有效消除因样品污染物或未知元素可能引起的测量误差。通过根据检测中已知生物分子的荧光强度对未知物的浓度进行数学量化,科学家可以可靠地确定目标分子的精确浓度水平。
传统荧光测定法的挑战
尽管传统荧光计具有众多优点,但仍然具有主要局限性:缺乏测定独立性。这些仪器通常是预先设计的,具有有限的激发和发射通道,从而限制了荧光测定的选择。然而,DeNovix 通过设计一种新型荧光计来应对这一挑战,改变了该领域。我们的荧光计配备了四个发射和激发通道,在选择荧光检测方法方面提供了灵活性。通过覆盖广泛的激发 (375 – 635 nm) 和发射 (435 –740 nm) 光谱,这些仪器支持一系列扩展的定量分析,适用于测量 dsDNA、ssDNA、RNA、蛋白质甚至定制的浓度水平化验。
DeNovix 荧光计简介
荧光计在科学研究和分析中发挥着至关重要的作用,能够在各个领域对生物分子进行精确定量。通过利用荧光原理,这些仪器提供高灵敏度测量,使科学家能够准确确定样品中核酸和蛋白质的浓度水平。
传统荧光计的灵活性一直受到限制,但我们 DeNovix 通过提供具有扩展检测选项的仪器,开创了荧光测定的新时代。借助我们先进的荧光计,研究人员可以探索更广泛的定量分析,确保实验中特异性和灵敏度。
在 DeNovix,我们制造专为研究应用量身定制的创新测量设备。我们为成为荧光测量仪器的供应商之一而感到自豪,我们提供荧光计技术,保证荧光测量中灵活性、灵敏度和可重复性。
DS-11系列
我们的DS-11 系列仪器将高动态范围荧光测定设备与微量吸光度能力相结合,为微升样品中的生物分子提供非常好检测。它们结构紧凑、易于使用,并允许进行全光谱紫外-可见分析和荧光,是快速核酸和蛋白质定量的理想选择。
QFX荧光计
我们提供的另一个解决方案是QFX 荧光计,适用于灵敏、可重复的荧光测定应用。它是另一种易于使用的仪器,提供直观的触摸屏界面,可实现无差错运行且无需设置。QFX 用于核酸和蛋白质定量,可与定制荧光应用程序配合使用以实现荧光团分析。与同类其他荧光计相比,QFX 在灵敏度、重现性和数据质量方面表现出色。